01 . Origine de l'accumulateur
Historique et théorie
Préambule :
Si le plomb a disparu dans le transport et la distribution de notre eau potable, il reste bien présent, pour des décennies, dans nos batteries d'accumulateurs au plomb .
Pour comprendre comment fonctionne votre batterie, il est important de savoir comment il a été possible de stocker de l'énergie électrique dans une boîte en plastique ! … alors que vous savez comment stocker (ou graver) des données sur un disque ou un support informatique .
Bref rappel historique :
Le premier accumulateur au plomb fut mis au point par le scientifique belge Monsieur Gaston Planté au XIXième siècle, en 1859 exactement : le 26 mars 1860, il présentera à l'Académie des Sciences, sa célèbre communication sur une "nouvelle pile secondaire d'une grande puissance" . (voir l'article sur Les découvertes )
On parlait déjà de " pile " car celle-ci fut découverte vers la fin du XVIIIième et c'est en 1800 que Monsieur Alessandro Volta en fit la première démonstration en réalisant un empilement d'éléments composés successivement d'une lame de zinc, d'une lame de feutre imbibée d'eau vinaigrée et d'une lame de cuivre . Il créa ainsi le premier dispositif de production électrochimique d'énergie électrique : la dénomination " pile " qui lui est attribuée trouve son origine dans la structure de ce " générateur " : un empilement de générateurs élémentaires .
Ensuite l'unité de tension (différence de potentiel) aux bornes de ces générateurs sera le Volt, en hommage à Alessandro Volta, à l'origine de la découverte de la pile voltaïque .
La grande découverte fut donc cette fameuse pile rechargeable ! … la différence entre une pile et un élément d'accumulateur est que la pile, une fois son énergie restituée, reste inutilisable alors que l'accumulateur aura la possibilité de régénérer ses plaques internes, de stocker de l'énergie et de fournir à nouveau un courant d'où la formulation de " pile secondaire d'une grande puissance " !
Le terme « accumulateur », employé pour un élément rechargeable, le distinguant ainsi de la pile (élément non rechargeable) est un générateur réversible : il peut stocker (accumuler) de l'énergie en convertissant l'énergie électrique en forme chimique, puis la restituer à tout moment sur demande en retransformant cette matière chimique en énergie électrique .
Ce processus serait quasiment " sans fin " s'il n'y avait pas la fatigue des éléments internes et leur détérioration .
Ce qui va suivre a été volontairement simplifié, pas de formules chimiques, pour que vous compreniez bien ce qui se passe à l'intérieur de votre bac quand vous branchez votre batterie 12 Volts sur votre installation ou/et quand vous rechargez celle-ci .
Cela vous aidera à mieux appréhender par la suite les divers symptômes rencontrés lors de l'existence de votre batterie d'accumulateurs tels que :
- élévation anormale de la température,
- déformation du bac,
- sulfatage des bornes,
- batterie ne tenant plus la charge,
- etc, etc ...
Fonctionnement d'un élément d'accumulateur :
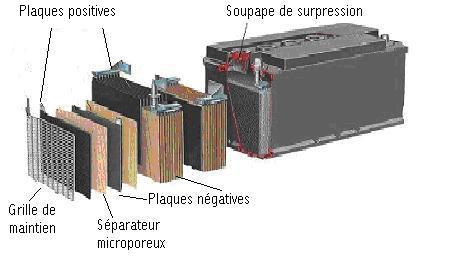
Un accumulateur au plomb élémentaire est constitué d'une plaque de plomb spongieux (Pb) et d'une plaque de bioxyde de plomb (PbO2) .
Quand ces plaques sont plongées dans une solution d'acide sulfurique (H2SO4), cet accumulateur est soumis à deux réactions chimiques différentes qui sont :
- la décharge lorsqu'un récepteur est raccordé sur ses bornes,
- la charge lorsqu'une tension externe est présente à ses bornes .
Explications :
a) Phénomène de décharge :
Quand deux électrodes, les deux plaques de plomb, sont plongées dans l'électrolyte (mélange d'eau distillée 65% et acide sulfurique 35%) et que l'on relie un récepteur aux bornes de l'accumulateur, entre le positif et le négatif, les réactions chimiques créent la circulation d'un courant électrique .
Ce courant électrique s'établit entre la plaque de bioxyde de plomb, appelée anode, et la plaque de plomb appelée cathode . ????????????????
Pendant cet état de décharge, le bioxyde de plomb de la plaque positive (anode) se transforme ????????????graduellement en sulfate de plomb (PbSO4) et le plomb spongieux de la plaque négative (cathode) se transforme ???????????également en sulfate de plomb .
Lorsque les plaques deviennent identiques, la même quantité de sulfate de plomb de part et d'autre, la différence de potentiel entre ces deux plaques s'annule et la circulation du courant s'interrompt : l'élément d'accumulateur est en situation de décharge profonde !
La quantité d'électricité circulant pendant une période de décharge déterminera la capacité de la batterie .(voir chapitre Les capacités)
En résumé, au cours de la décharge :
Anode (+) : - le bioxyde de plomb diminue, - le sulfate de plomb augmente,
Cathode (-) : - le plomb diminue, - le sulfate de plomb augmente,
Electrolyte : - le % d'eau augmente, = 85% - le % d'acide diminue, = 15%
b) Phénomène de charge :
Afin de recharger l'accumulateur, il faut relier les bornes de l'accumulateur à celles d'une source de tension continue (chargeur de batterie) : la borne de la source de tension à la borne de l'accumulateur (anode), celui-ci devenant récepteur vis-à-vis de la source de tension .
Le sens de circulation du courant électrique pendant la charge est l'inverse du sens de circulation de la situation de décharge .
Le sulfate de plomb présent sur les deux plaques est dissous par le passage du courant et les plaques reprennent leur état initial .
Le phénomène chimique serait "sans fin", s'il n'y avait pas la fatigue des éléments internes et leur détérioration .
En résumé, au cours de la charge :
Anode ( ) : - le bioxyde de plomb augmente, - le sulfate de plomb diminue,
Cathode (-) : - le plomb augmente, - le sulfate de plomb diminue,
Electrolyte : - le % d'eau diminue, - le % d'acide augmente .
Conclusions :
1 . Pendant la décharge de l'élément accumulateur (qui correspond à l'utilisation de votre batterie : éclairage, réfrigérateur, etc...) la réaction chimique forme des cristaux de sulfate de plomb insolubles qui cristallisent dans les pores des plaques de l'accumulateur .
Au niveau de l'électrolyte, la concentration d'acide diminue fortement : si vous mesurez la densité de l'électrolyte à l'aide d'un pèse-acide avant (sur une batterie chargée) et après (sur une batterie en décharge ou totalement déchargée), vous trouverez des valeurs très différentes .
2 . Pendant la charge de l'élément accumulateur (mise en charge par votre panneau solaire ou votre chargeur secteur) la réaction chimique se fait essentiellement autour de la reconstitution d'acide sulfurique autour des électrodes .
Conséquences :
Lors d'une charge après une décharge relativement profonde, une importante quantité d'acide sera reconstituée au niveau des plaques . Cet acide concentré se mettra à suinter vers le fond de votre batterie . Généralement, vers 90% de la phase de recharge, la partie basse des éléments contient de l'électrolyte concentré et la partie haute de la cuve, de l'électrolyte dilué : on dit que l'électrolyte est stratifié .
Arrêter la charge à ce stade aurait des conséquences désastreuses, à savoir un fonctionnement hétérogène des électrodes, menant à une fatigue rapide de leur partie inférieure, d'où l'importance de s'équiper d'un excellent régulateur de charge au niveau de votre panneau solaire et d'un chargeur de batterie de grande qualité voire de type IUoU .
Les 10 derniers % de recharge sont les plus importants, ceux sont eux qui vont conditionner la durée de vie de votre batterie .
La phase finale de la charge est dite « de surcharge » .
C'est la phase pendant laquelle le courant se partage en un courant de charge proprement dit et en un courant d'électrolyse .
L'électrolyse c'est quoi ? … ici on parle de l'électrolyse du liquide se trouvant dans la partie haute de la cuve : l'électrolyse de l'eau est un procédé qui décompose l'eau en créant de l'oxygène et de l'hydrogène lorsqu'elle est traversée par un courant électrique .
(voir chapitre Processus d'autodécharge )
Ce courant d'électrolyse produira de l'oxygène à l'électrode positive et de l'hydrogène à l'électrode négative . L'intérêt de ce processus étant de se rapprocher le plus possible de l'état de charge complète de l'accumulateur mais aussi, grâce au dégagement gazeux dans la cuve, de réhomogénéiser la concentration de l'électrolyte puisque l'électrolyte concentré se trouve en partie basse de la cuve .
Cette réhomogénéisation de l'électrolyte est la principale fonction à assurer en fin de charge . Elle est nécessaire à chaque charge, sous peine d'entraîner un fonctionnement hétérogène des électrodes menant à une réduction importante de leur durée de vie .
Si vous avez bien compris le processus de fonctionnement de cet élément d'accumulateur, vous saurez déceler par la suite les anomalies pouvant survenir sur votre batterie .
(voir chapitre suivant Le fonctionnement des batteries )
Rappel des découvertes
Historique de la batterie d'accumulateurs
Dû à son applicabilité universelle, l’énergie électriques joue un rôle prépondérant dans la technologie d’aujourd’hui.
" L’inconvénient ": De toute évidence nous avons besoin de l'électricité. Il ne peut pas être entreposé ou ne peut être créé par de simples appareils; il doit être obtenu directement d'une centrale électrique. La quantité d'énergie électrique qui peut être emmagasinée directement, i.e. dans les condensateurs, est si petite qu'elle peut seulement être utilisée dans les applications où une très faible demande est exigée pour compenser des interruptions d'alimentation électrique. Par conséquent, pour que l'énergie électrique soit conservée, elle doit être convertie sous une autre forme d'énergie.
Les batteries, aussi appelée " accumulateurs ", sont des réservoirs d'énergie électrochimiques qui utilisent les propriétés chimiques pour le stockage. Dans cet historique, nous verrons une vue d'ensemble des systèmes du stockage. Nous commencerons avec l'historique de l'emmagasinage d'énergie électrochimique et la naissance de la batterie d'accumulateurs acide/plomb.
Historique sur l'emmagasinage d'énergie électrochimique
Les premières recherches scientifiques coïncident au tout début du développement des systèmes du stockage d'énergie électrochimiques . Des noms tels que Luigi Galvani (1737 à 1798) et Alessandra Cont di Volta (1745 à 1827) sont associés à ces découvertes et existent aujourd'hui sous des termes tel que " galvanisation " et " voltage ".
Dans ses expériences, Luigi Galvani a remarqué que la patte d'une grenouille morte se contractait quand elle entrait en contact avec deux métaux différents . Il conclue qu'il y a un rapprochement entre l'électricité et l'activité musculaire . Volta orienta ses recherches sur les effets produits quand différents métaux entrent en contact avec des solutions salines . Il empila des plaquettes de cuivre et de zinc en alternance et inséra un morceau de carton trempé d'une solution saline entre chaque plaquette . Cette " batterie voltaïque " ou " organe électrique artificiel " comme s'amusa à décrire Volta, fourni de l'électricité quand les plaquettes furent reliées à des fils conducteurs . Des recherches supplémentaires, confirmèrent rapidement la corrélation entre les réactions chimiques et l'énergie électrique.
Dans la foulée des recherches sur le plomb/acide sulfurique/bioxyde de plomb un système a été découvert : La batterie d'accumulateurs acide/plomb . Ce système a été utilisé pour emmagasiner l'électricité pour les télégraphes, par Gaston Planté (1834 à 1889) en 1859 . Ils utilisèrent des plaquettes de plomb en guise d'électrodes . Ils ont obtenu une certaine capacité aux fils des charges/décharges répétées . Ces batteries n'étaient cependant pas adaptées à une production industrielle .
À la fin du 19e siècle, la recherche pour développer des accumulateurs électrochimiques a évolué rapidement . La dynamo et l'ampoule ont été inventées et, dû aux développements industriels, le besoin d'emmagasiner l'énergie électrique augmenta . La production industrielle de batteries d'accumulateurs acide/plomb débuta autour de1880, quand Émile Alphonse Faure demanda un brevet pour la fabrication de plaquettes enduites d'une pâte pour les batteries d'accumulateurs acide/plomb .
Les premiers balbutiements de la batterie d'accumulateurs acide/plomb
Autour de 1880, Émile Alphonse Faure a développé un processus pour couvrir les deux côtés d'une plaquette de plomb d'une pâte composée de poudre de plomb et d'acide sulfurique . Cela signifiait que ce " soi-disant " dispositif pourrait contenir, particulièrement, une grosse capacité dès la première charge . Ce fut une percée considérable qui mena la batterie acide/plomb directement à sa fabrication industrielle . Plusieurs compagnies spécialisées sont apparues, y compris S. A. La Force et, la Lumière, pour laquelle William Thomson, devenu plus tard Lord Kelvin of Largs, a travaillé comme ingénieur associé . L'échelle de température absolue fut nommée en son nom .
Au début, les plans furent conçus pour construire de gros accumulateurs d'énergie électrique pour les fournisseurs d'électricité . À la demande de la ville de Buffalo, W. Thompson a établi un plan pour alimenter la ville avec de l'électricité provenant des chutes Niagara . Il généra 80,000 volts et alimenta Buffalo avec une batterie de 40,000 cellules . Branchées par groupes de 50 cellules, elles alimentèrent les maisons d'une tension de 100 volts .
Cependant, les cellules de Faure dans lesquelles les électrodes positives et négatives étaient enroulées en spirale démontrèrent une faible durabilité aux cycles de charge/décharge . Par conséquent, ce fut l'échec des premières tentatives de fabrication en industrie .
En 1881, M. Sellon a demandé un brevet pour un procédé qui consiste à appliquer la pâte sur une plaquette perforée plutôt qu'une plaquette lisse . Il améliora considérablement plus l'adhérence que Faure . Sellon utilisa de l'antimoine comme matière . Parallèlement, Volkmar développa une procédure similaire qui consistait à utiliser une grille de plomb . Alors la plaquette formée d'une grille était inventée et bientôt testée et appliquée à une gamme de variantes . Aussi en 1881 C. Brush fait une demande de brevet pour une électrode de plomb à grande surface mais ondulée . C'était le signe avant-coureur de la plaquette à grande surface utilisée aujourd'hui .
Un autre type de plaquette qui joue encore un rôle important aujourd'hui qui était aussi disponible : la plaquette tubulaire ou plaquette blindée . Sous cette forme, une tige de plomb traverse le centre d'un tube (normalement) de 8 mm de diamètre et sert à dévier le courant . L'adhérence de la matière active est obtenu en utilisant un revêtement externe . Des composants différents sont donc utilisés pour dériver le courant et stabiliser la structure mécanique . Résultat de cette configuration : plusieurs cycles de charge/décharge et un plus haut niveau d'utilisation effective de la matière active . Au début, les tubes étaient emboîtés et composés de caoutchouc dur . Après la deuxième guerre mondiale, la fibre de verre tressées, matière tissée de verre et de fibres artificielles, la matière purement artificielle ou matière non-tissée (polyester), entrèrent dans la composition des tubes .
L'élément primaire :
En 1786, le biologiste Luigi Galvani a disséqué une grenouille. A chaque fois que le scalpel en acier de Galvani touchait un crochet en cuivre, qui tenait en place la cuisse de la grenouille, celle-ci se contractait. Galvani pensa que cette énergie provenait de l'animal et l'a donc appelée "électricité animale".
L'ami et associé de Galvani, Alessandro Volta, n'était pas d'accord avec cette idée. Il était convaincu que l'électricité avait été générée par les deux différents métaux dans un milieu humide. Des expériences ont ensuite confirmé cette idée et en 1797, Volta conçut la vraie première batterie : la pile voltaïque. La pile était composée de 49 paires de disques de cuivre et de zinc, disposés alternativement, séparés par un tissu trempé dans de l'eau salée. Et lorsque les deux extrémités étaient connectées à un conducteur, le courant passait.
Dans une pile voltaïque, l'électricité est générée par une réaction chimique et lorsqu'elle est épuisée, la pile ne peut pas être rechargée. Cela s'appelle un élément primaire.
L'élément secondaire :
Dans une pile voltaïque, l'électricité est générée par une réaction chimique et lorsqu'elle est épuisée, la pile ne peut pas être rechargée. Cela s'appelle un élément primaire.En 1803, le physicien allemand Johann Wilhelm Ritter a conçu une pile voltaïque à l'envers. La pile de Ritter se composait de disques en cuivre uniquement, séparés de couches de substance à base de carton trempé dans une solution saline. La colonne de Ritter pouvait accumuler de l'énergie électrique, mais en aucun cas la produire. Cela s'appelle un élément secondaire, batterie de stockage ou accumulateur. L'électricité nécessaire à la charge de la pile de Ritter pouvait seulement être obtenue par une source de courant primaire, telle qu'une pile voltaïque. Cela rendait la découverte de Ritter intéressante certes, mais peu pratique d'utilisation.
1854 a marqué une étape importante dans le développement de l'électricité. Le médecin et scientifique allemand Joseph Sinsteden plaça deux plaques en plomb dans un bac contenant de l'acide sulfurique dilué. Cet acide sulfurique réagit avec la surface des plaques et forma une couche de sulfate de plomb. Sinsteden connecta les plaques à une source de courant primaire et constata qu'une couche d'oxyde de plomb se formait sur une plaque, tandis que du plomb spongieux se formait sur l'autre. Après cette charge, la batterie pouvait à nouveau être déchargée : il y avait un courant non inférieur à 2 V : ce qui représentait bien plus que ce que les prédécesseurs de Sinsteden, Volta et Ritter, avaient jamais pu réaliser. Pendant la décharge du sulfate de plomb se formait sur les deux plaques, exactement comme lors de la première fois. Ainsi, le processus pouvait redémarrer. La batterie plomb/acide venait de voir le jour !
La plaque Planté
En se basant sur les travaux de Sinsteden, le scientifique belge Planté développa en 1861 la première batterie secondaire à usage pratique, dans laquelle les plaques en plomb étaient roulées en bobines et séparées par des bandes de feutre.
Dans l'élément de Planté, nous reconnaissons tout l'équipement de la batterie plomb/acide existant de nos jours : de l'acide sulfurique dilué dans lequel sont plongées deux plaques en plomb, couvertes de sulfate de plomb. La feuille de plomb sert uniquement de conducteur, car le vrai processus a lieu sur le sulfate de plomb et c'est pour cela qu'il est appelé "masse active". La préparation de la plaque en plomb, en permettant la création du sulfate de plomb, est appelée "formation".
La formation des plaque de Planté fut une tâche longue et difficile. Avant que ne ce soit formé assez de sulfate de plomb sur la plaque ne plomb, il fallait qu'elle se charge et se décharge de manière réitérée. Cela pouvait prendre des semaines, et parfois même des mois, avant d'obtenir la capacité souhaitée.
En 1881, la plaque de Planté fut améliorée par Charles Francis Brush. Il appliqua de l'oxyde de plomb sur des plaques, qui avaient été incisées, fendues ou perforées, en introduisant l'oxyde en fine poudre dans les cavités. Cette méthode représente encore la base de la plaque de Planté actuelle.