08 . Le processus d'autodécharge
L'autodécharge des batteries au plomb
Les batteries au plomb sont soumises à de phénomènes d'auto-décharge . L’origine de l’autodécharge provient des réactions secondaires se produisant au niveau des électrodes . Ces réactions secondaires sont nombreuses et plus ou moins prépondérantes les unes par rapport aux autres . En outre, ces réactions secondaires ne sont pas encore toutes identifiées par la communauté scientifique . Nous présentons ci-après une d’entre elles .
Les oxydants et les réducteurs :
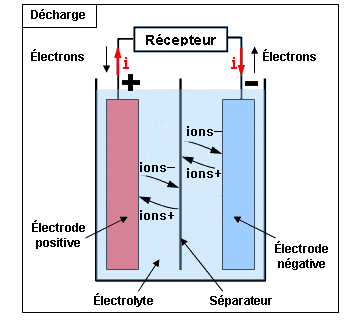
Par réaction électrochimique, le courant électrique est produit par la circulation d'électrons entre 2 plaques ou électrodes :
-
une électrode positive ou plaque positive composée d'un corps oxydant, capable d'attirer des électrons,
-
une électrode négative ou plaque négative composée d'un corps réducteur, capable de céder des électrons.
Une batterie ou une pile se caractérise donc tout d'abord par un couple «oxydant-réducteur», (par exemple Plomb/Oxyde de plomb, Nickel/Cadmium...) échangeant des électrons. L'association de deux plaques constitue l'entité primaire d'une batterie.
Les deux plaques baignent dans une solution électrolytique (ou électrolyte), liquide ou sous forme de gel. C'est la réaction entre la solution et les électrodes qui est à l'origine du déplacement des électrons et des ions dans la solution. Ainsi, l'électrolyte a pour fonction d'assurer la conduction ionique et, plus généralement, de participer à la réaction chimique.
Un isolant poreux (ou séparateur) permet de séparer les deux plaques tout en autorisant le passage des ions.
a) les oxydants
b) les réducteurs
Au niveau de chaque électrode, des réactions d’oxydoréductions peuvent se produire naturellement . En effet, l’anode constituée de plomb (Pb) peut réagir avec les ions H3O+ présents dans l’électrolyte . Egalement, la cathode composée d’oxyde de plomb (Pb02) peut réagir avec l’eau H20 présente dans l’électrolyte .
Chacune de ces réactions se produisent au niveau des électrodes entre des oxydants et des réducteurs sans transport de charge à travers l’électrolyte. Les matériaux actifs des électrodes y participent.
A la cathode : L’eau de l’électrolyte est oxydée dégageant du dioxygène gazeux (O2) et 2 électrons. Ces deux électrons sont directement exploités par l’oxyde de plomb (PbO2) de la cathode. Le plomb (Pb) est alors réduit en ions Pb2+.
A l’anode : Le plomb (Pb) est oxydé en ions Pb2+ libérant 2 électrons. Ces deux électrons sont directement consommés par les ions H3O+. Les ions H3O+ sont alors réduits dégageant du dihydrogène gazeux (H2).
De ce fait, l'électrolyse de l'eau induit une baisse de performance pendant la décharge car une partie des électrons produits par la réaction principale sert à enclencher l’électrolyse de l’eau et non à alimenter les charges électriques.
Egalement, lorsque la batterie est déconnecté, la tension induite par les électrodes est suffisante pour forcer l'électrolyse de l'eau et provoquer ainsi l'auto-décharge.
L'auto-décharge d'une batterie présente donc deux conséquences préjudiciables :
Lorsque la batterie est déconnectée (circuit ouvert), elle s'auto-décharge.
Ainsi, une batterie chargée qui ne serait pas sollicité se retrouve complètement déchargée au bout de plusieurs mois.
Nous donnons ci-dessous les temps d'auto-décharge typique d'une batterie au repos (en circuit ouvert) en fonction de la température ambiante :
 Temps d'auto-décharge des batteries au plomb en fonction de la température ambiante. Les batteries au plomb s'auto-décharge d'autant plus vite que la température ambiante est élevée. Le taux d'auto-décharge des batteries actuelles, en terme de perte de capacité, est réduit en moyenne entre 2 % et 5 % par mois (à 20°C).
Temps d'auto-décharge des batteries au plomb en fonction de la température ambiante. Les batteries au plomb s'auto-décharge d'autant plus vite que la température ambiante est élevée. Le taux d'auto-décharge des batteries actuelles, en terme de perte de capacité, est réduit en moyenne entre 2 % et 5 % par mois (à 20°C).
- La capacité de la batterie diminue. En effet, même lorsque la batterie alimente un récepteur électrique, les réactions secondaires se produisent.
L' électrolyse de l'eau :
L’électrolyse de l’eau est une réaction chimique forcée faisant intervenir les deux couples oxydants-réducteurs suivants :
La réaction d’oxydoréduction naturelle est décrite ci-après :
L’oxydant le plus fort est le dioxygène (O2). Celui-ci va se réduire eau (H2O) selon la demi-équation de réduction suivante :
De même, le réducteur le plus fort est le dihydrogène (H2). Celui-ci va s’oxyder en l’ion H+ selon la demi-équation d’oxydation suivante :
On obtient la réaction d'oxydo-réduction suivante :
Ainsi, en présence de dihydrogène et de dioxygène, ces deux éléments réagissent pour former de l’eau. Cette réaction chimique est naturelle.
La réaction inverse n’est pas naturellement possible. Si nous souhaitons décomposer l’eau en dioxygène et dihydrogène, il est nécessaire de forcer la réaction à l’aide d’un courant électrique. Pour cela, on utilise un générateur qui va forcer le passage des électrons dans le sens inverse. C'est ce qu'on appelle l'électrolyse de l'eau.